Tutto quello che c’è da sapere sulla solidificazione dell’acqua, ovvero il passaggio dallo stato liquido a quello solido. Ecco una guida completa.
L’acqua è una sostanza che gioca un ruolo fondamentale per la vita sulla Terra. Una delle sue caratteristiche più interessanti è la sua capacità di passare dallo stato liquido a quello solido a una temperatura di 0 gradi Celsius. In questo articolo, esploreremo il motivo per cui l’acqua congela a questa temperatura e approfondiremo la scienza che si cela dietro questo fenomeno.
La struttura molecolare dell’acqua
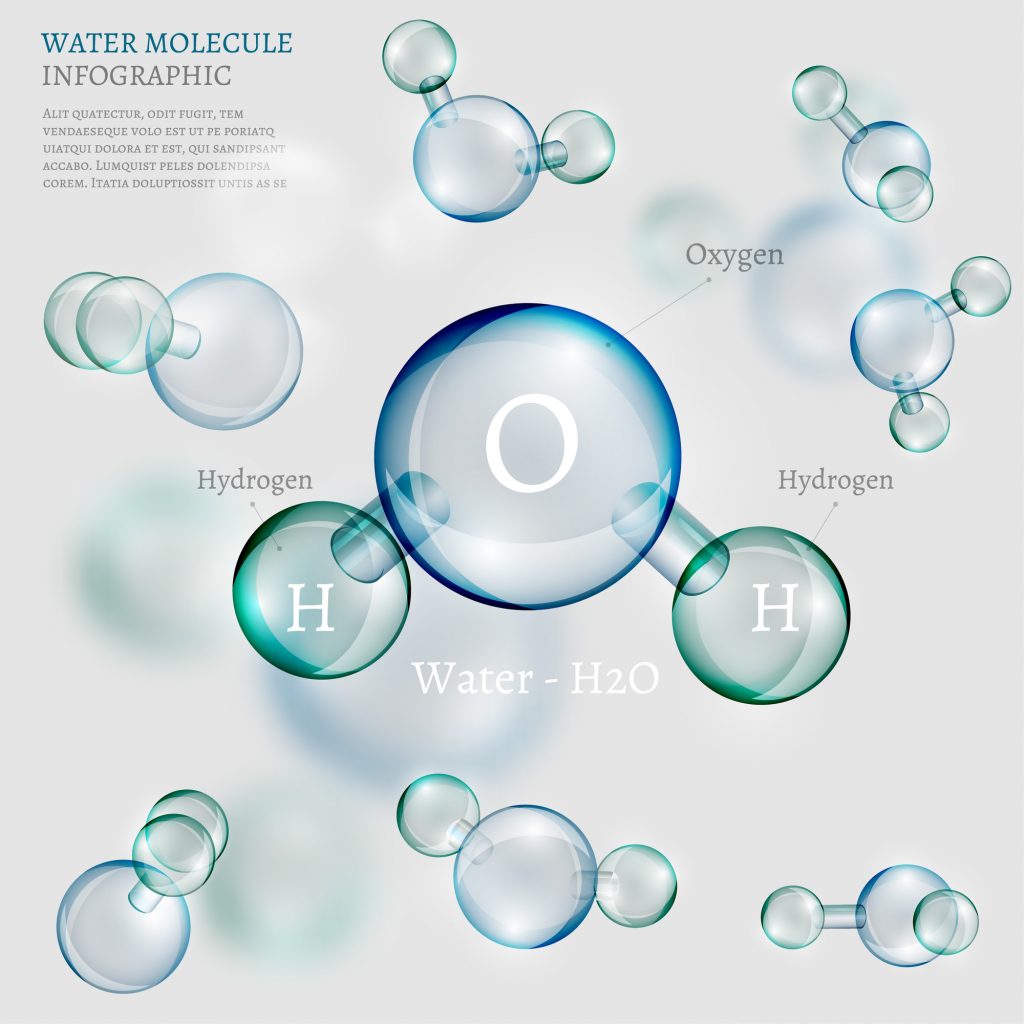
Per comprenderne il processo di solidificazione (o congelamento), è essenziale esaminare la sua struttura molecolare. L’acqua è composta da molecole di due atomi di idrogeno e uno di ossigeno (H2O). Queste molecole sono polari, il che significa che c’è una distribuzione asimmetrica di carica. L’ossigeno attira gli elettroni, creando una regione leggermente negativa attorno all’ossigeno e regioni leggermente positive attorno agli atomi di idrogeno.
I legami idrogeno
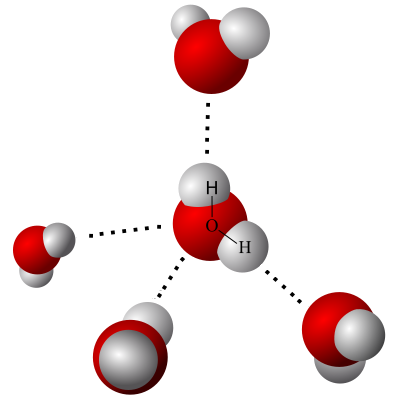
A temperatura ambiente, l’acqua è liquida grazie a questi legami che mantengono le molecole insieme. Tuttavia, quando la temperatura scende, questi legami diventano più stabili e organizzati, portando all’ordinamento delle molecole e al passaggio dalla fase liquida a quella solida.
Il punto di congelamento
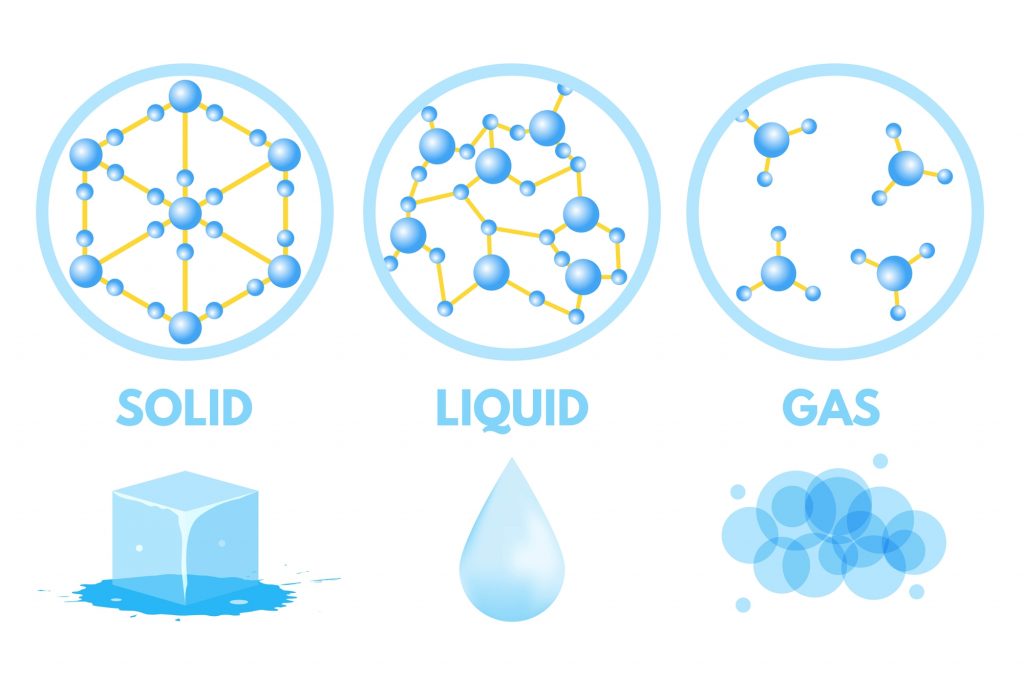
Il punto di congelamento dell’acqua, ovvero 0 gradi Celsius (o 32 gradi Fahrenheit), è una costante fisica. Questo valore è basato su condizioni standard di pressione atmosferica al livello del mare. Quando raggiunge questa temperatura, le molecole si organizzano in una struttura cristallina, dando origine al ghiaccio che noi tutti conosciamo.
Il ruolo della pressione atmosferica
Va sottolineato che il punto di congelamento può variare in base alla pressione atmosferica. Ad esempio, a quote più elevate, dove la pressione atmosferica è inferiore, l’acqua può congelare a temperature inferiori a 0 gradi Celsius. Questo fenomeno è spesso sfruttato in montagna, dove la cottura di cibi richiede temperature di ebollizione più basse a causa della minore pressione.
Applicazioni pratiche
Questo passaggio dallo stato liquido a solido lo sperimentiamo spesso nella vita quotidiana. Dal mantenimento degli alimenti freschi nel congelatore di casa, all’uso di antigelo nei motori delle automobili: poter controllare la solidificazione dell’acqua ci è di grande aiuto e ci aiuta a semplificare la nostra vita.
Cose che cambiano il punto di congelamento
È interessante notare che aggiungere sostanze disciolte all’acqua può influenzare il suo punto di congelamento. Ad esempio, il sale da cucina disciolto in pentola abbassa il suo punto di congelamento, consentendo all’acqua di rimanere liquida a temperature inferiori. Questo principio è sfruttato per sciogliere il ghiaccio sulle strade durante l’inverno.
La fisica della solidificazione
La solidificazione dell’acqua è un processo complesso guidato dalla fisica molecolare. Quando si raffredda, le molecole perdono energia cinetica. A temperature inferiori, i legami idrogeno diventano più forti, portando alla formazione di strutture cristalline in cui le molecole sono disposte in modo ordinato. Questo processo richiede energia, che viene rilasciata quando l’acqua congela.
